文獻摘要: Enhancing interpretability of AI with radiomics based deep neural network proof of concept in the classification of Parkinsonian syndromes with 18F FDG PET imaging
Objectives
本研究提出了一種放射組學引導的雙通道深度神經網路 (RDDNN),旨在提高使用 18F-FDG PET 影像分類帕金森氏症候群 (IPD、MSA、PSP) 的可解釋性和可重現性。RDDNN 整合了來自擴張型卷積網路的局部特徵和基於 Transformer 自注意力網路的全域特徵。它透過多層次的可解釋性(特徵整合、SHAP 值量化以及基於注意力的視覺化,如 Layer-CAM 和 Rollout Attention Map (RAM))提升了特徵透明度和臨床理解。該框架提供了一個臨床上可解釋且可重現的解決方案,其診斷性能可與人類專家媲美,同時顯著提高了效率。
Methodology
本研究使用了來自華山醫院的 1,498 名受試者(中國隊列)和來自慕尼黑大學醫院的 90 名帕金森氏症患者(德國隊列)的雙中心數據集。18F-FDG PET 影像經過預處理,包括正規化至 MNI 空間、平滑、SUVR 計算和 Z-score 正規化。RDDNN 模型採用雙通道架構:一個局部通道使用擴張型卷積網路 (dilated convolutional networks) 進行細粒度特徵提取,另一個全域通道使用 Transformer 框架捕捉長距離上下文依賴關係。 放射組學特徵(從 20 個 ROI 提取 2,140 個)使用 Pyradiomics 提取。三階段特徵選擇策略(方差過濾、Elastic Net-regularized LASSO 迴歸和 Pearson 相關分析)將特徵減少至 8 個穩定的放射組學特徵和 10 個深度學習衍生的潛在特徵。分類採用 XGBoost 分類器。可解釋性透過 SHAP 評估特徵重要性,Layer-CAM 用於基於 CNN 的局部路徑,RAM 用於基於 Transformer 的全域通道,並使用 BrainNet Viewer 視覺化 3D 注意力圖。可重現性則透過 SHAP 值和 t-SNE 視覺化在不同隊列間進行 Pearson 相關分析評估。
放射組學特徵(從 20 個 ROI 提取 2,140 個)使用 Pyradiomics 提取。三階段特徵選擇策略(方差過濾、Elastic Net-regularized LASSO 迴歸和 Pearson 相關分析)將特徵減少至 8 個穩定的放射組學特徵和 10 個深度學習衍生的潛在特徵。分類採用 XGBoost 分類器。可解釋性透過 SHAP 評估特徵重要性,Layer-CAM 用於基於 CNN 的局部路徑,RAM 用於基於 Transformer 的全域通道,並使用 BrainNet Viewer 視覺化 3D 注意力圖。可重現性則透過 SHAP 值和 t-SNE 視覺化在不同隊列間進行 Pearson 相關分析評估。
Results
在內部盲測隊列中,RDDNN 模型實現了高性能,AUC 為 0.99,準確度為 0.98。在外部測試隊列中,它保持了穩健的性能,AUC 為 0.94,準確度為 0.81。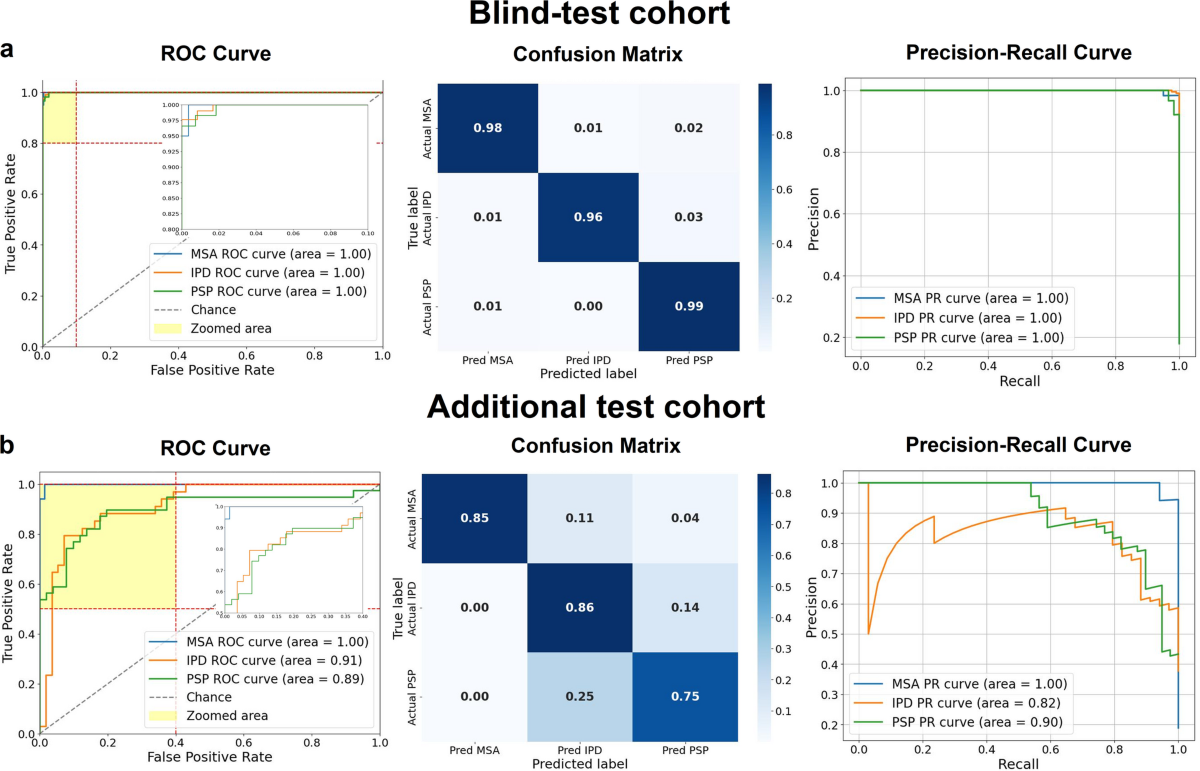 SHAP 和相關性分析表明,跨通道的資訊具有互補性和臨床可解釋性,且不同隊列間的 SHAP 特徵重要性排名具有高度一致性 (Pearson’s r=0.98–0.99, p<0.001)。Layer-CAM 和 RAM 的熱圖顯示,疾病特異性激活發生在解剖學相關區域(例如,PSP/MSA 的中腦、殼核、尾狀核),與已知的代謝缺陷一致。與核醫學專家相比,模型顯著縮短了評估時間 (p<0.001),減少了 80% 以上,並在評估機率方面表現出更高的穩定性。
SHAP 和相關性分析表明,跨通道的資訊具有互補性和臨床可解釋性,且不同隊列間的 SHAP 特徵重要性排名具有高度一致性 (Pearson’s r=0.98–0.99, p<0.001)。Layer-CAM 和 RAM 的熱圖顯示,疾病特異性激活發生在解剖學相關區域(例如,PSP/MSA 的中腦、殼核、尾狀核),與已知的代謝缺陷一致。與核醫學專家相比,模型顯著縮短了評估時間 (p<0.001),減少了 80% 以上,並在評估機率方面表現出更高的穩定性。
Discussions
RDDNN 框架為帕金森氏症候群的分類提供了一個強大的雙通道方法,並在兩個不同隊列中進行了驗證,這顯著增強了其泛化能力。整合多種可解釋性工具(SHAP、Layer-CAM、RAM)是一個顯著優勢,為模型決策和解剖學合理性提供了寶貴的見解。相較於人類專家,模型在效率上的提升突顯了其臨床應用潛力。然而,研究承認存在局限性,包括由於訓練樣本有限而限制了更複雜深度學習網路的使用,這表明需要使用更大數據集進行進一步驗證。該框架目前的驗證僅限於 FDG-PET 影像,其在其他影像模態中的有效性需要進一步研究。此外,儘管模型表現出更高的穩定性,但在外部測試隊列中,其在區分 MSA 疾病方面不如核醫學專家有效,這表明未來有改進的空間。 未來的研究也應專注於開發本質上可解釋的模型架構,而不是僅僅依賴於事後解釋。